牛血清白蛋白對人肝微粒體UGT2B7代謝齊多夫定的影響
汪洋 高潔 喬海靈(鄭州大學醫(yī)學院臨床藥理研究所 河南鄭州 450052)
?
牛血清白蛋白對人肝微粒體UGT2B7代謝齊多夫定的影響
汪洋 高潔 喬海靈
(鄭州大學醫(yī)學院臨床藥理研究所 河南鄭州 450052)
【摘要】目的 研究牛血清白蛋白對人肝微粒體尿苷二磷酸葡萄糖醛酸轉(zhuǎn)移酶(uridine-5'-diphosphate glucuronosyl-transferase,UGT)2B7代謝活性的影響?方法 采用差速離心法制備人肝微粒體,以齊多夫定(3'-疊氮-3'-脫氧胸苷)為探針,考察人肝微粒體孵育體系中UGT2B7代謝活性,采用反相高效液相色譜法測定齊多夫定及其代謝物濃度?孵育體系分為兩組,分別為對照組和牛血清白蛋白組(含2%的牛血清白蛋白)?結(jié)果 在兩種人肝微粒體反應(yīng)體系中,UGT2B7代謝齊多夫定的動力學行為均符合米曼式方程?對照組和牛血清白蛋白組齊多夫定的酶動力學參數(shù)如下:Vmax分別為(1 359.0±135.8)和(1 268.4±300.1)pmol/(min·mg protein),Km分別為(368.0±64.3)和(111.4±6.9)μM,CLint分別為(3.7±0.4)和(11.4±2.7)μl/(min·mg protein)?與對照組相比,牛血清白蛋白組的Km顯著降低(P<0.05),CLint明顯升高(P<0.05)?結(jié)論 牛血清白蛋白可顯著影響人肝微粒體反應(yīng)體系UGT2B7催化活性,使UGT2B7代謝齊多夫定的Km降低?CLint升高?
【關(guān)鍵詞】牛血清白蛋白;人肝微粒體;尿苷二磷酸葡萄糖醛酸轉(zhuǎn)移酶2B7;齊多夫定
人尿苷-5'-二磷酸葡萄糖醛酸轉(zhuǎn)移酶(UGTs)是催化內(nèi)源性和外源性物質(zhì)葡萄糖醛酸化的膜結(jié)合酶?葡萄糖醛酸結(jié)合反應(yīng)是一種普遍的Ⅱ相代謝反應(yīng),在此反應(yīng)中UGTs催化尿苷-5'-二磷酸葡萄糖醛酸(UDPGA)與親脂性底物結(jié)合,化合物的親水性增加,促進其排泄,是機體重要的解毒途徑之一?人類迄今發(fā)現(xiàn)至少19種具有功能的UGTs,根據(jù)核苷酸序列的相似性分為4個家族:UGT1?UGT2?UGT3和UGT8[1],其中UGT1?UGT2在化學物質(zhì)進行Ⅱ相生物轉(zhuǎn)化時起主要作用?UGT2B7系UGT2B家族重要成員,在肝臟中含量較為豐富?UGT2B7不僅催化內(nèi)源性化合物如雄甾酮?雌三醇?膽酸?類維生素A,也參與催化許多臨床藥物如非甾體抗炎藥?麥考酚酸?齊多夫定?可待因?貝特類等,同時也是唯一催化嗎啡類的Ⅱ相代謝酶[2]?
體外代謝實驗可有效排除體內(nèi)諸多因素的干擾,有利于直接觀察肝藥酶對底物的選擇性代謝,為進一步的整體實驗提供可靠的理論依據(jù)?人肝微粒體?人肝細胞?重組肝藥酶等體外系統(tǒng)已成功用于體內(nèi)肝臟藥物代謝研究的預(yù)測?目前,利用在人肝微粒體體系獲得的酶動力學研究結(jié)果如酶動力學參數(shù)(如Km和Vmax)及抑制常數(shù)(Ki)等,預(yù)測體內(nèi)的葡萄糖苷酸化程度也是比較常用的體外預(yù)測體內(nèi)的方法之一?但Lit-tle等[3]研究發(fā)現(xiàn)人肝微粒體中富含的亞麻酸和花生四烯酸等長鏈不飽和脂肪酸是UGT2B7的底物,在UGT2B7代謝其他底物時,脂肪酸可競爭性抑制UGT2B7的活性,導致體外預(yù)測的UGT2B7活性遠遠小于其體內(nèi)的實際活性?Rowland等[4]研究發(fā)現(xiàn)人肝微粒體反應(yīng)體系中加入牛血清白蛋白,可減小脂肪酸的抑制作用,致UGT2B7 Km降低,CLint顯著增加,從而提高體外實驗預(yù)測的準確性?經(jīng)過一系列研究,Row-land提出“牛血清白蛋白效應(yīng)"理論,即牛血清白蛋白可消除人肝微粒體反應(yīng)體系中長鏈不飽和脂肪酸對UGTs的競爭性抑制作用,提高預(yù)測體內(nèi)藥物清除率的準確性?目前國內(nèi)尚無關(guān)于牛血清白蛋白對人肝微粒體中UGT2B7活性影響的報道?
齊多夫定口服吸收良好,主要經(jīng)肝臟中UGT2B7催化失活,生成齊多夫定葡萄糖苷酸?齊多夫定是體內(nèi)?體外研究UGT2B7活性公認的探針,可通過研究其在人肝微粒體孵育系統(tǒng)的固有清除率來推測人體內(nèi)的清除率?本研究國內(nèi)首次考察了牛血清白蛋白對正常人肝微粒體UGT2B7代謝齊多夫定的影響,以期為準確預(yù)測體內(nèi)藥物代謝提供理論和實驗依據(jù)?
1 材料與方法
1.1 試驗藥物和試劑 牛血清白蛋白(BSA,Sigma公司,批號1001116884,CAS 9048-46-8,純度≥98%);尿苷二磷酸-α-D-葡萄糖醛酸(UDP-GA,三鈉鹽,Sigma公司,批號1001595481,CAS63700-19-6,純度98%~100%);丙甲菌素(批號063M4008V,CAS27061-78-5,純度≥98%);齊多夫定(3'-疊氮-3'-脫氧胸苷,廈門邁克制藥有限公司,批號031102,純度>99%);齊多夫定-β-D-葡萄糖苷酸(Toronto Research Chemicals Inc,批號A825050);磷酸二氫鉀(天津市凱通化學試劑有限公司,分析純,純度≥99.5%);磷酸氫二鉀(天津市風船化學試劑科技有限公司,分析純,純度≥99.0%);氯化鎂(北京北伐精細化學品有限責任公司);高氯酸(天津市鑫源化工廠,純度70.0%~72.0%);EDTA(湖南湘中地質(zhì)實驗研究所);甲醇(天津市四友精細化學品有限公司,批號433722-05126,色譜純,純度≥99.9%);乙腈(天津市四友精細化學品有限公司,批號432079-06517,色譜純,純度≥99.9%);異丙醇(天津市光復科技發(fā)展有限公司,分析純,純度≥99.7%);蔗糖(天津市風船化學試劑科技有限公司,分析純);無水乙醇(天津市登科化學試劑有限公司,分析純,純度≥99.7%);磷酸(天津市科密歐化學試劑有限公司,色譜純,純度≥85.0%);鹽酸(洛陽市化學試劑廠,分析純,純度36.0%~38.0%)?實驗用水均為超純水?
1.2 儀器 美國安捷倫HP1100高效液相色譜分析系統(tǒng),二極管陣列檢測器,自動進樣器,美國安捷倫公司生產(chǎn);6L-88B型旋渦混合器,海門市其林貝爾儀器制造有限公司;HH.W21.420型電子恒溫水箱,北京市光明醫(yī)療儀器廠;賀利氏低溫高速離心機(Kendro La-boratory Products);Milpore超純水系統(tǒng)?
1.3 治療方法
1.3.1 人肝微粒體的制備與蛋白濃度的測定 收集肝血管瘤患者肝標本6例,年齡30~67歲,男性4例,女性2例,吸煙史?飲酒史患者均為2例,近期均未使用影響UGT酶活性的藥物,肝功能均正常?本試驗方案經(jīng)鄭州大學醫(yī)學倫理委員會批準,受試者簽署知情同意書?肝臟標本收集后立即用預(yù)冷的Tris-HCl緩沖液洗滌,濾紙將水分吸干,分裝至凍存管中,液氮保存?
采用差速離心法制備HLMs?所用試劑和器材均于4℃預(yù)冷?液氮保存的肝臟于冰上解凍,稱重,加入相當于3倍肝臟重量的重懸液1(含0.15 M KCl,0.002 M EDTA),制備肝勻漿?將肝勻漿置于離心管中,9 000 g離心20 min(4℃),取上清液?將上清液100 000 g離心60 min(4℃)?棄上清,加入Tris-HCl緩沖液(0.15 M,pH7.6)洗滌1次,100 000 g離心60 min(4℃)?所得沉淀用磷酸鹽緩沖液(含0.21 mol/L蔗糖,pH7.4)重懸,分裝,-80℃保存待用?Bradford法測定微粒體蛋白濃度?
1.3.2 齊多夫定標準溶液的配制 精密稱取0.267 2 g齊多夫定標準品于10 ml容量瓶中,用甲醇溶解,定容,得100 mM的齊多夫定標準液?準確吸取5 ml該標準液至10 ml容量瓶中,用甲醇定容,得50 mM標準液?分別依次用甲醇倍比稀釋成濃度為25 000?12 500?6 250?3 125?1 560?780?390和195μM的齊多夫定標準溶液?
1.3.3 孵育反應(yīng) 兩種孵育體系總體積均為100μl?對照組:PBS(50μM,pH=7.4,0%牛血清白蛋白),微粒體蛋白(0.2 mg/ml),丙甲菌素(50μg/mg蛋白),蔗糖(0.25 M)?牛血清白蛋白組:PBS(50μM,pH=7.4,2%牛血清白蛋白),其余組分相同?事先加入系列濃度的齊多夫定標準液于氮氣(室溫)下吹干?在37℃預(yù)孵育5 min,加入UDPGA(5 mM)啟動反應(yīng),孵育時間為60 min?
1.3.4 樣品處理及色譜條件 樣品處理孵育60 min后,冰浴加入高氯酸10μl終止反應(yīng),渦旋混勻30 s,離心10 min(12 000 rpm),取上清75μl,15μl進樣?色譜條件色譜柱:Diamonsil C18柱(5μm,250 mm× 4.6 mm,5μm);柱溫:30℃;流動相為乙腈:磷酸鉀緩沖液(20 mM,pH=2.2)=12∶88(v/v);流速:1.0 ml/min,二極管陣列檢測器,波長266 nm;進樣量15μl?
1.3.5 人肝微粒體中齊多夫定葡萄糖苷酸標準曲線制備 取10 mg齊多夫定葡萄糖苷酸(95%),溶于1 ml超純水中,得20 844.5μM的儲備液?依次倍比稀釋,得一系列濃度的齊多夫定葡萄糖苷酸標準液:10 422.3?5 211.2?2 605.6?1 302.8?651.4?325.7? 162.8?81.4?40.7?20.4和10.2μM?
分別于孵育體系中加入系列濃度的齊多夫定葡萄糖苷酸對照品10μl(不加UDPGA),使其濃度分別為1.02?2.04?4.07?8.14?16.28?32.57?65.14和130.28μM,按照“1.3.4樣品處理及色譜條件"項下步驟操作?記錄樣品峰面積(A),樣品峰面積對齊多夫定葡萄糖苷酸濃度(C)作回歸曲線?
1.3.6 酶活性的測定 以探針藥物的轉(zhuǎn)化程度(Turnover)作為酶活性指標,具體表示為TR [pmol/(min·mg)]=(△C×1000)/(B×T),其中△C為代謝產(chǎn)物齊多夫定葡糖苷酸濃度(μM),B為微粒體蛋白的濃度(mg/ml),T為孵育時間(min)?
1.3.7 人肝微粒體孵育條件的優(yōu)化 最適孵育時間的確定:體系加入UDPGA啟動反應(yīng),分別于37℃孵育20?40?60?80?100和120 min,考察孵育時間對齊多夫定代謝的影響?最適蛋白濃度的確定:于反應(yīng)體系中加入不同蛋白濃度0.1?0.2?0.3?0.4?0.6和0.8 mg/m l,考察微粒體蛋白濃度對齊多夫定代謝的影響?
1.3.8 人肝微粒體齊多夫定酶動力學參數(shù)的測定反應(yīng)體系中底物齊多夫定的濃度分別為19.5?39.0?78.0?156.0?312.5?625.0和1 250.0μM,以代謝產(chǎn)物的生物轉(zhuǎn)化程度(TR)為反應(yīng)速度?
1.4 統(tǒng)計學處理 采用Prism 5.0進行齊多夫定葡萄糖苷酸的酶動力學參數(shù)Km?Vmax和CLint的計算?統(tǒng)計學分析均由SPSS 17.0軟件包完成?對照組與牛血清白蛋白組UGT2B7代謝的酶動力學參數(shù)采用配對t檢驗進行比較,P<0.05為差異有統(tǒng)計學意義?
2 結(jié)果
2.1 方法學考察
2.1.1 專屬性 在本實驗條件下,齊多夫定葡萄糖苷酸有較大的色譜峰,肝微粒體中的雜質(zhì)?齊多夫定的色譜峰不干擾樣品峰,在該色譜條件下,齊多夫定葡萄糖苷酸?齊多夫定的保留時間分別為8.2?20.2 min左右(見圖1),說明該方法的專屬性較高?
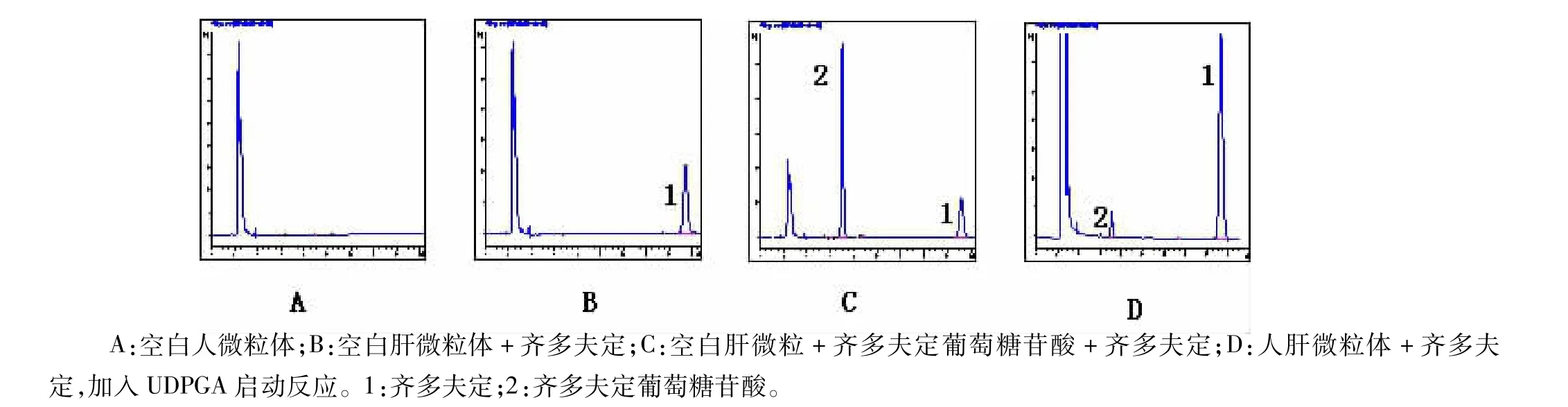
圖1 人肝微粒體中齊多夫定及其代謝物的高效液相色譜圖
2.1.2 標準曲線 以齊多夫定葡萄糖苷酸樣品峰面積對濃度作回歸曲線,得方程為C=0.120 9A+0.080 7(r=1),表明齊多夫定葡萄糖苷酸在10.2~130.28μM范圍內(nèi)線性良好?該方法的靈敏度為10.2μM?
2.1.3 精密度和相對回收率 該方法的批間?批內(nèi)RSD分別為1.10%~3.66%和1.07%~3.84%,均小于5%;齊多夫定葡萄糖苷酸的相對回收率為100.05%~103.15%(表1)?結(jié)果表明,本實驗方法的精密度和相對回收率均符合生物樣品分析要求?
2.1.4 人肝微粒體孵育時間和蛋白濃度的選擇 考察齊多夫定葡萄糖苷酸生成量與孵育時間關(guān)系的結(jié)果顯示,孵育時間為60 min時,齊多夫定葡萄糖苷酸生成量較大,因此選擇孵育時間為60min(圖2-A)?考察齊多夫定葡萄糖苷酸的生成量與蛋白濃度關(guān)系的結(jié)果表明,蛋白濃度在0.1~0.8 mg/ml范圍內(nèi)齊多夫定葡萄糖苷酸生成的量與蛋白濃度基本呈線性?綜合實驗條件,在保證檢測靈敏度的情況下,本實驗選擇微粒體蛋白濃度為0.2 mg/ml(圖2-B)?
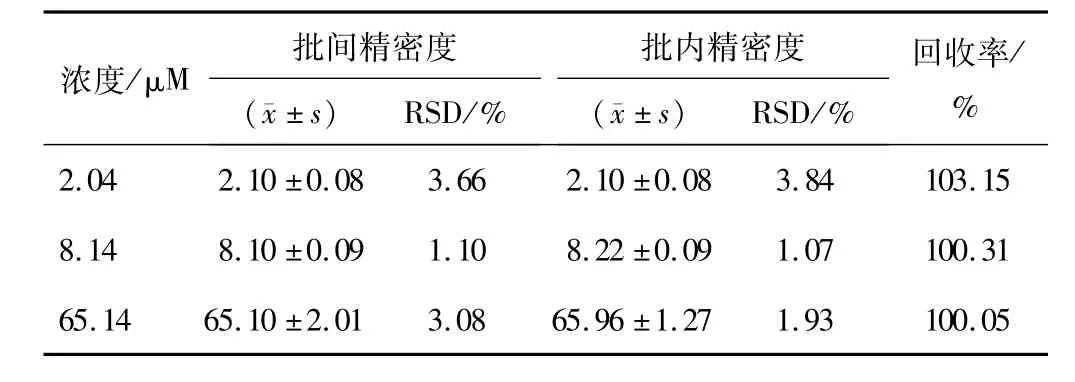
表1 精密度和相對回收率(n=5)
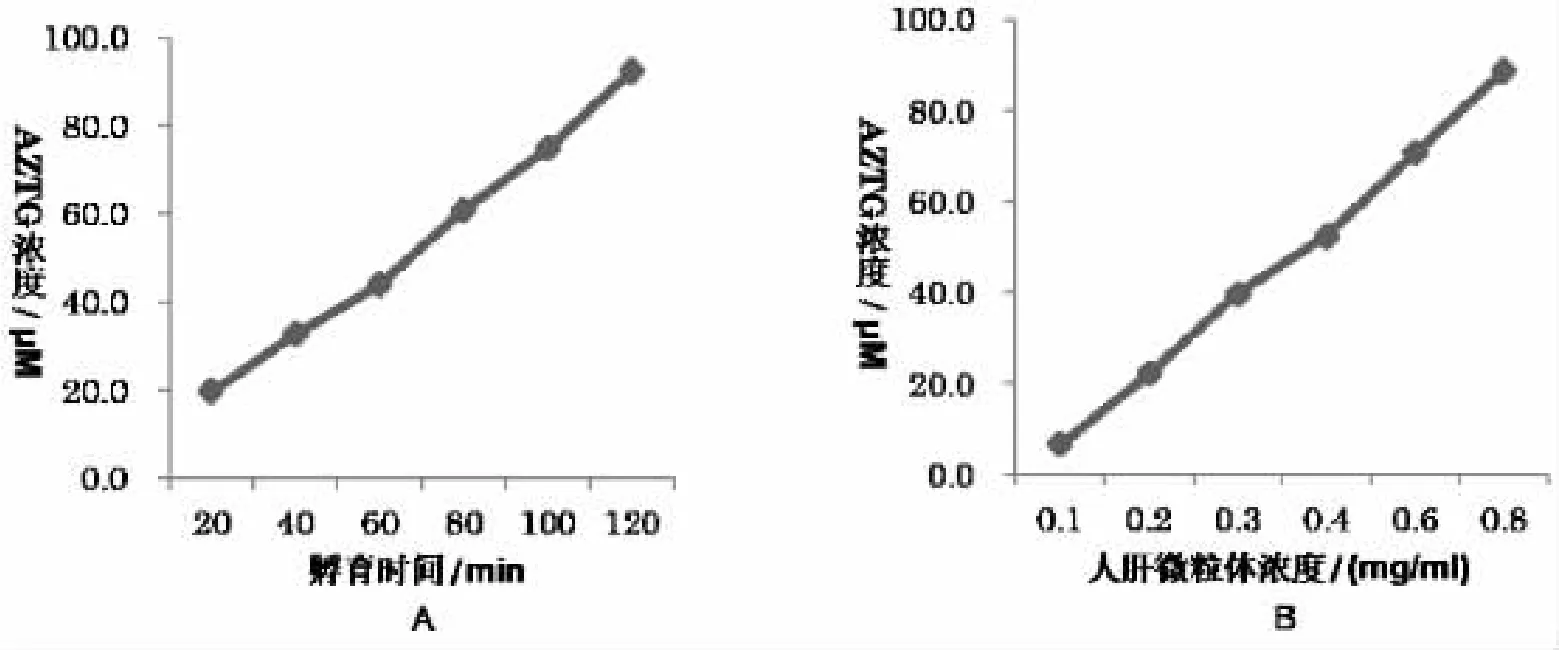
圖2 人肝微粒體孵育時間(A)和蛋白濃度(B)對齊多夫定代謝的影響
2.2 牛血清白蛋白對UGT2B7代謝活性的影響 人肝微粒體反應(yīng)體系中齊多夫定葡萄糖苷酸的酶動力學符合米曼氏方程,對照組和牛血清白蛋白組的酶動力學參數(shù)見表2?與對照組相比,牛血清白蛋白組UGT2B7代謝齊多夫定的Km顯著性降低(P<0.05),CLint顯著性升高(P<0.05)?結(jié)果表明,牛血清白蛋白顯著影響人肝微粒體中UGT2B7的催化活性?
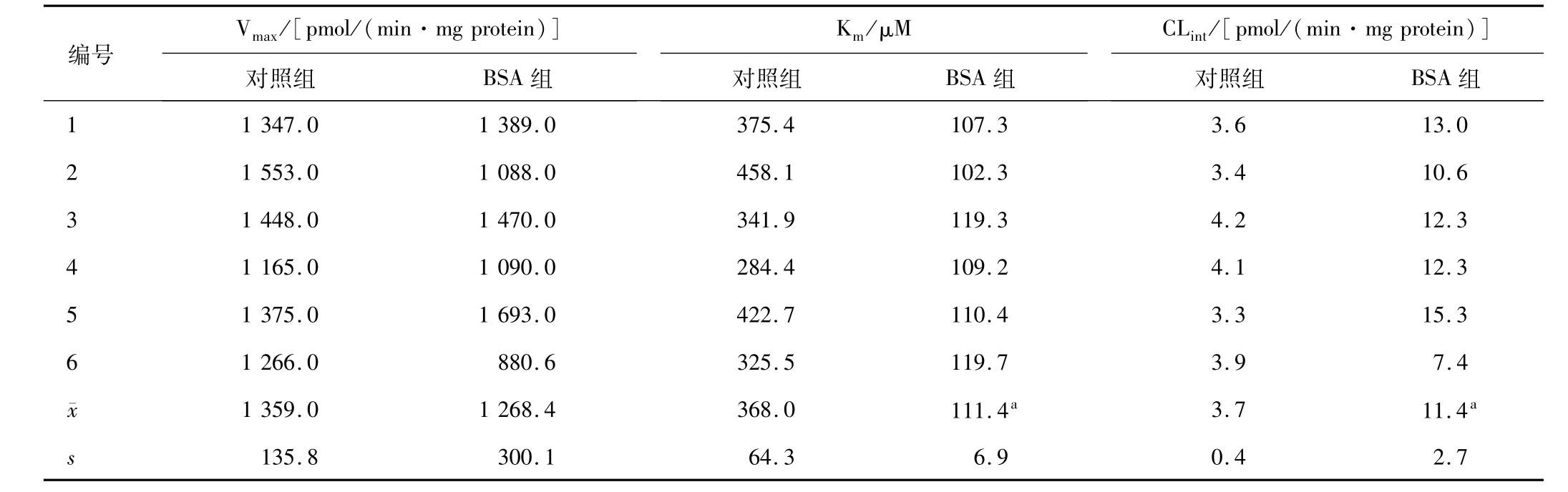
表2 人肝微粒體中齊多夫定葡萄糖苷酸藥動學參數(shù)(n=6)
3 討論
藥物在人體內(nèi)肝臟代謝清除率的體外預(yù)測已經(jīng)日趨成熟,可通過體外研究數(shù)據(jù)估算藥物體內(nèi)的代謝清除率?目前,人源性肝細胞和肝微粒體的可獲得性,人肝細胞由新鮮制備到冷凍保存,使人體內(nèi)藥物肝臟代謝清除率體外預(yù)測的準確性得到很大改善?但藥物代謝清除率的預(yù)測還存在一些問題?Lwatsubo等[5]對25種不同化合物的體內(nèi)外清除率進行比較,發(fā)現(xiàn)50%的預(yù)測值與實測值相比誤差在3倍范圍之內(nèi),而70%的結(jié)果在5倍誤差范圍之內(nèi)?
Uchaipichat等[6]體外研究發(fā)現(xiàn),藥物葡萄糖苷酸化過程獲得的酶動力學參數(shù)(如Km和Vmax)及抑制常數(shù)(Ki)也常常低估體內(nèi)的葡萄糖苷酸化程度?肝微粒體中的亞麻酸?亞油酸和花生四烯酸等長鏈不飽和脂肪酸可被UGT2B7催化代謝生成其葡萄糖苷酸化產(chǎn)物?當UGT2B7催化代謝其他化合物時,長鏈不飽和脂肪酸會競爭性抑制UGT2B7的活性?Nenad等[7]采用UGT2B7重組酶和混合人肝微粒體研究發(fā)現(xiàn),牛血清白蛋白可影響UGT2B7的催化活性?Miners等[8-9]報道體外反應(yīng)體系中的牛血清白蛋白可使UGT2B7的活性明顯增強,加入牛血清白蛋白,Km約降低了一個數(shù)量級,顯著提高了預(yù)測的準確性?因此研究經(jīng)UGT2B7代謝的藥物時,人肝微粒體中加入牛血清白蛋白可消除長鏈不飽和脂肪酸對UGT2B7的抑制作用,提高體外代謝實驗預(yù)測體內(nèi)藥物清除率的準確性?
Michael等[10]研究證實,齊多夫定比嗎啡?可待因更適合作為UGT2B7的特異性探針?齊多夫定是一種有效的核苷類逆轉(zhuǎn)錄酶抑制劑,可有效抑制病毒復制,降低艾滋病的傳染性,重建患者的免疫功能,其在體內(nèi)經(jīng)UGT2B7催化生成齊多夫定葡萄糖苷酸?本研究以齊多夫定為探針,在國內(nèi)首次報道了牛血清白蛋白對人肝微粒體中UGT2B7代謝活性的影響?研究發(fā)現(xiàn)微粒體反應(yīng)體系中加入2%的牛血清白蛋白后,UGT2B7代謝齊多夫定的酶動力學參數(shù)發(fā)生改變,Km明顯降低(P<0.05),CLint顯著升高(P<0.05)?證實牛血清白蛋白消除了反應(yīng)體系中固有存在的抑制劑對UGT2B7的抑制作用,進而增強了其代謝活性?因此研究UGTs參與代謝的藥物,尤其是UGT2B7參與代謝的藥物,進行人肝微粒體代謝實驗應(yīng)加入一定量的牛血清白蛋白,使實驗結(jié)果盡可能準確地反映體內(nèi)藥物代謝過程?
本研究還在國內(nèi)首次建立了人肝微粒體中齊多夫定葡萄糖苷酸的高效液相測定方法?齊多夫定在266 nm處存在最大吸收峰,在此波長條件下,齊多夫定葡萄糖苷酸也存在很強的吸收,且孵育體系中的其他物質(zhì)不干擾樣品峰,最終確定檢測波長為266 nm?曾嘗試采用甲醇-水作為流動相,在此條件下,雖然齊多夫定峰形良好,但齊多夫定葡萄糖苷酸的色譜峰拖尾非常嚴重?因此考察了乙腈-磷酸鹽緩沖液(20 mM, pH=2.2)流動相及不同比例對分離效果的影響,發(fā)現(xiàn)乙腈-磷酸鹽緩沖液比例為12∶88時兩種物質(zhì)的分離度和柱效均比較理想,故加以選用?實驗結(jié)果證明,本研究建立的人肝微粒體中齊多夫定葡萄糖苷酸的高效液相色譜測定方法,操作簡便?靈敏度高?重現(xiàn)性好?專屬性強,為UGT2B7的體外活性測定奠定了基礎(chǔ)?
參考文獻
[1] Mackenzie P,Bock K W,Burchel B,et al.Nomenclature update for the mammalianUDP glucuronosyltransferase(UGT)gene superfamily[J].Pharmacogenet Genomics,2005,15(10):677-685.
[2] Rowland A,Miners JO,Mackenzie P I.The UDP-glucuronosyltrans-ferase:their role in drugmetabolism and detoxification[J].Int JBio-chem Cel Biol,2013,45(6):1121-1132.
[3] Litle JM,Kurkela M,Sonka J,et al.Glucuronidation of oxidized faty acids and prostaglandinsB1 and E2 by human hepatic and recombinant UDP-glucuronosyltransferases[J].J Lipid Res,2004,45(7):1694-1703.
[4] Rowland A,Eliot D J,Knights K M,et al.The“albumin efect"and in vitro-in vivo extrapolation:sequestration of long chain unsaturated faty acids enhances phenytoin hydroxylation by human liver micro-somal and recombinant cytochrome P450 2C9[J].DrugMetab Dispos,2008,36:870-877.
[5] Lwatsubo T,Hirota N,Ooie T,etal.Prediction of in vivo drugmetabo-lism in the human liver from in vitrometabolism data[J].Pharmacol Ther,1997,73(2):147-171.
[6] Uchaipichat V,Winner L K,Mackenzie P I,et al.Quantitative Predic-tion of in vivo inhibitory interactions involving glucuronidated drugs from in vitro data:the efect of fluconazole onzidovudine glucuronida-tion[J].Br JClin Pharmacol,2006,61:427-439.
[7] Nenad M,Paolo SM,JariY K,etal.Bovine Serum Albumin Decreases Km Values of Human UDP-Glucuronosyltransferases 1A9 and 2B7 and Increases Vmax Values of UGT1A9[J].Drug Metab Dispos,2011,39(11):2117-2129.
[8] Miners JO,Knights K M,Houston JB,etal.In vitro-in vivo correla-tions for drugs and other compounds eliminated by glucuronidation in humans:pitfals and promises[J].Biochem Pharmacol,2006,71(11):1531-1539.
[9] Miners JO,Mackenzie P L,Knights K M.The prediction of drug-glu-curonidation parameters in humans:UDP-glucuronosyltransferase en-zyme-selective substrate and inhibitor probes for reaction phenotyping and in vitro-in vivo extrapolation of drug clearance and drug-drug in-teraction potential[J].Drug Metab Rev,2010,42(1):196-208.
[10]Michael H,Soundarajan K,Qin H,et al.Evaluation of 3'-azido-3'-deoxythymidine,morphine,and codeine as probe substrates for UDP-glucuronosyltransferase 2B7(UGT2B7)in human livermicrosomes:specificity and influence of the UGT2B7*2 polymorphism[J].Drug Metab Dispos,2003,31(9):1125-1133.
Effects of bovine serum album in on zidovudine glucuronidated by UGT2B7 in human liver m icrosomes
Wang Yang,Gao Jie,Qiao Hailing
(Department of Clinical Pharmacology,School of Medicine,Zhengzhou University,Zhengzhou 450052,China)
【Abstract】Objective To investigate the efect of bovine serum albumin(BSA)on the activities of UDP-glucuronosyltrans-ferase(UGT)2B7 in human livermicrosomes(HLMs).M ethods HLMswere prepared by diferential centrifugationmethods.The kinetics of glucuronidation of zidovudine(AZT,3'-azido-3'-deoxy-thymidine),a selective UGT2B7 substrate,was measured to reflect the activity of UGT2B7 in HLMs.The formations of AZT and itsmetabolite,AZT-β-D-glucuronide,were analyzed using a reversed-phase high-performance liquid chromatography.Incubation systems were divided into two groups.One was control group and the other was BSA group which included 2%BSA.Results UGT2B7-dependent AZT glucuronida-tion in control and BSA groups showed that the results were consistent with a typical Michaelis-Menten equation.The enzyme kinetics parameters of AZT in controland BSA groupswere as folows:the Vmaxwere(1 359.0±135.8)and(1 268.4±300.1)pmol/(min·mg protein),the Kmwere(368.0±64.3)and(111.4±6.9)μM,the CLintwere(3.7±0.4)and(11.4± 2.7)μl/(min·mg protein),respectively.Compared with control group,the Kmvalue of UGT2B7 was significantly decreased and the CLintvalue was significantly increased in the BSA group (P<0.05).Conclusion The activity of UGT2B7 in HLMs wasbook=11,ebook=17significantly influenced by BSA which decreased the value of Kmand increased the value of CLint.
【Key words】bovine serum albumin;Human livermicrosomes;UGT2B7;zidovudine
(收稿日期:2015-09-01)
通訊作者:喬海靈,E-mail:qiaohl@zzu.edu.cn?
【中圖分類號】R 96
doi:10.3969/j.issn.1004-437X.2016.01.002

